Neostigmina
| Neostigmina | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
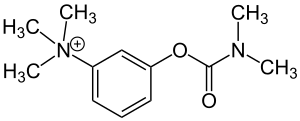
| Formula bruta o molecolare | C12H19N2O2 |
| Massa molecolare (u) | 223,294 |
| Numero CAS | |
| Codice ATC | N07 |
| PubChem | 5824 |
| DrugBank | DBDB01400 |
| SMILES | CN(C)C(=O)OC1=CC=CC(=C1)[N+](C)(C)C |
| Dati farmacocinetici | |
| Metabolismo | Idrolisi del carbammato e N-demetlazione cui segue glucuronidazione.[1] |
| Emivita | 50-90 minuti |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 300 - 310 - 315 - 317 - 319 - 330 - 334 - 335 |
| Consigli P | 260 - 264 - 280 - 284 - 301+310 - 302+350 [2] |
La neostigmina è un farmaco parasimpaticomimetico con funzione di inibitore dell'acetilcolinesterasi reversibile.
Chimica
[modifica | modifica wikitesto]La neostigmina fu sintetizzata per la prima volta nel 1931 da Aeschlimann e Reinert.[3] È sintetizzata a partire dal 3-dimetilamminofenolo che, fatto reagire con l'N-dimetilcarbamoil cloruro, forma il relativo dimetil-carbammato. Il prodotto è successivamente metilato con dimetilsolfato a dare la neostigmina come sale metilsolfato, approvato per uso parenterale mentre per via orale viene impiegato il bromuro.[4]
Strutturalmente è un derivato di semplificazione molecolare della fisostigmina, un alcaloide con la stessa attività caratterizzato da un gruppo aril-carbammato.[1] In particolare la distanza fra la testa ammonica quaternaria e l'estere è simile a quella di acetilcolina e fisostigmina.
Farmacocinetica
[modifica | modifica wikitesto]La neostigmina è priva di attività a livello centrale in quanto avendo un atomo di azoto che forma un sale d'ammonio è permanentemente carica e non può superare la barriera emato-encefalica.
La biodisponibilità orale è bassa a causa dello scarso assorbimento a livello gastrointestinale, e pertanto quando la neostigmina è somministrata per via orale sono richieste dosi significativamente maggiori rispetto alla somministrazione parenterale (15–30 mg o più per via orale contro gli 0,5-2 per via parenterale).[5]
Inoltre a causa del rapido metabolismo per idrolisi del carbammato, l'emività plasmatica è breve e conseguentemente l'intervallo tra le somministrazioni è generalmente di 2-4 ore.
Farmacodinamica
[modifica | modifica wikitesto]La neostigmina è un inibitore reversibile dell'acetilcolinesterasi (AChE) della classe degli arilcarbammati. L'acetilcolinesterasi è l'enzima che catalizza l'idrolisi del legame estereo dell'acetilcolina a dare colina e acetato. L'inibizione dell'AChE da parte degli anticolinesterasici impedisce o riduce la degradazione dell'acetilcolina, aumentandone quindi le concentrazioni a livello sinaptico. Poiché nell'ambito della trasmissione colinergica la degradazione del neurotrasmettitore è il principale meccanismo d'interruzione della trasmissione del segnale, l'inibizione dell'AChE provoca effetti di agonismo colinergico.
In particolare la neostigmina agisce a livello del sito attivo dell'AChE dove l'idrolisi del carbammato va a transesterificare un residuo di serina della tasca catalitica. Si ottiene così l'enzima carbammoilato dal quale la rigenerazione della forma attiva è molto più lenta (nell'ordine di grandezza dei minuti) rispetto al ritorno alla forma attiva in seguito ad acetilazione (meccanismo fisiologico che avviene in seguito all'idrolisi del legame estereo dell'acetilcolina), che richiede meno di un millisecondo.[1] L'acetilcolina, avendo il suo sito recettoriale occupato, non viene degradata e perciò ne vengono aumentate le concentrazioni sinaptiche. Poiché nell'ambito della trasmissione colinergica il fattore principale che determina l'interruzione del segnale non è il riassorbimento del neurotrasmettitore ma la sua degradazione ad opera dell'AChE, l'inibizione di tale enzima consente un'aumentata attività colinergica.
Usi
[modifica | modifica wikitesto]Viene usata abitudinariamente in anestesia al termine degli interventi chirurgici per invertire gli effetti dei rilassanti neuromuscolari quali il vecuronio. La neostigmina può trovare applicazioni nella ritenzione urinaria post-chirurgica derivante dagli anestetici generali e per trattare la tossicità dei curari.
Viene utilizzata come terapia palliativa nella cura della Miastenia gravis.
Un'altra indicazione per l'uso è la gestione conservativa della pseudo-ostruzione colica acuta, o sindrome di Ogilvie, in cui i pazienti ottengono una dilatazione del colon massiccia in assenza di una vera ostruzione meccanica.[6]
Gli ospedali a volte somministrano una soluzione contenente neostigmina per via endovenosa per ritardare gli effetti dell'avvelenamento da morso di serpente. Alcuni risultati di ricerca promettenti sono stati riportati anche per la somministrazione nasale del farmaco come trattamento per il morso di serpente.[7]
Effetti avversi
[modifica | modifica wikitesto]La neostigmina può indurre effetti collaterali oculari generici tra cui: mal di testa, dolore alla fronte, visione offuscata, facododesi, iniezione pericorneale, irite congestizia, varie reazioni allergiche e, raramente, distacco della retina. [8]
La neostigmina causa un rallentamento della frequenza cardiaca (bradicardia); per questo motivo viene generalmente somministrato insieme a un farmaco parasimpaticolitico come atropina o glicopirrolato. [9]
I sintomi gastrointestinali si verificano subito dopo l'ingestione e includono anoressia, nausea, vomito, crampi addominali e diarrea.
Note
[modifica | modifica wikitesto]- ^ a b c Foye, p. 413.
- ^ Sigma Aldrich; rev. del 26.07.2012 riferita al bromuro di neostigmina (CAS )
- ^ David M. Whitacre, Reviews of Environmental Contamination and Toxicology, Springer, 2008, p. 298, ISBN 978-0-387-73162-9.
- ^ GandG.
- ^ GandG, cap. 10.
- ^ Nell Maloney e H. David Vargas, Acute Intestinal Pseudo-Obstruction (Ogilvie's Syndrome), in Clinics in Colon and Rectal Surgery, vol. 18, n. 2, 2005-5, pp. 96–101, DOI:10.1055/s-2005-870890. URL consultato il 24 aprile 2020.
- ^ Tommaso C. Bulfone, Stephen P. Samuel e Philip E. Bickler, Developing Small Molecule Therapeutics for the Initial and Adjunctive Treatment of Snakebite, in Journal of Tropical Medicine, vol. 2018, 30 luglio 2018, DOI:10.1155/2018/4320175. URL consultato il 24 aprile 2020.
- ^ Gilman, Goodman & Gilman 1980, p. 114..
- ^ Gilman, Goodman & Gilman 1980, p. 109..
Bibliografia
[modifica | modifica wikitesto]- (EN) Laurence Brunton, et al., Goodman and Gilman's Manual of Pharmacology and Therapeutics, McGraw-Hill Professional, 28 settembre 2007, p. 642, DOI:10.1036/0071443436, ISBN 978-0-07-144343-2.
- William O. Foye, Thomas L. Lemke; David A. Williams, Principi di chimica farmaceutica, 5ª ed., Padova, Piccin, maggio 2011, p. 1498, ISBN 978-88-299-2034-1.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto]Wikimedia Commons contiene immagini o altri file su Neostigmina
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) neostigmine, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.