Fosfatidiletanolamina: diferenças entre revisões
m Bot: removendo {{sem-fontes}}, artigo contém notas de rodapé |
m manutênção refs. |
||
| Linha 1: | Linha 1: | ||
{{info/Química |
|||
{{chembox new |
|||
| ImageFile = Phosphatidyl-ethanolamine.svg |
| ImageFile = Phosphatidyl-ethanolamine.svg |
||
| ImageSize = |
| ImageSize = |
||
| Linha 26: | Linha 25: | ||
Por exemplo, a fosfatidilcolina e fosfatidiletanolamina tem colina e etanolamina nos seus grupos-cabeça polares. Em todos esses compostos, o grupo-cabeça esta ligado ao [[glicerol]] por um fosfodiéster, no qual o [[grupo fosfato]] tem uma carga negativa em [[pH]] neutro. O álcool polar pode estar negativamente carregado (como no fosfatidillinositol 4,5 bifosfato), neutro (fosfatidilserina) ou positivamente carregado (fosfaticilcolina, fostatidiletanolamina). Essas cargas tem uma contribuição significante nas propriedades de superfície das membranas. |
Por exemplo, a fosfatidilcolina e fosfatidiletanolamina tem colina e etanolamina nos seus grupos-cabeça polares. Em todos esses compostos, o grupo-cabeça esta ligado ao [[glicerol]] por um fosfodiéster, no qual o [[grupo fosfato]] tem uma carga negativa em [[pH]] neutro. O álcool polar pode estar negativamente carregado (como no fosfatidillinositol 4,5 bifosfato), neutro (fosfatidilserina) ou positivamente carregado (fosfaticilcolina, fostatidiletanolamina). Essas cargas tem uma contribuição significante nas propriedades de superfície das membranas. |
||
A S-Adenosil metionina pode subsequentemente metilar a amina de fosfatidiletanolaminas para produzir fosfatidilcolinas. Pode encontrar-se principalmente na região interna (citoplasmática) da bicamada lipídica.<ref>{{Citar periódico|ultimo=Wellner|primeiro=Niels|ultimo2=Diep|primeiro2=Thi Ai|ultimo3=Janfelt|primeiro3=Christian|ultimo4=Hansen|primeiro4=Harald Severin|data= |
A S-Adenosil metionina pode subsequentemente metilar a amina de fosfatidiletanolaminas para produzir fosfatidilcolinas. Pode encontrar-se principalmente na região interna (citoplasmática) da bicamada lipídica.<ref>{{Citar periódico|ultimo=Wellner|primeiro=Niels|ultimo2=Diep|primeiro2=Thi Ai|ultimo3=Janfelt|primeiro3=Christian|ultimo4=Hansen|primeiro4=Harald Severin|data=março 2013|titulo=N-acylation of phosphatidylethanolamine and its biological functions in mammals|jornal=Biochimica Et Biophysica Acta|volume=1831|numero=3|paginas=652–662|issn=0006-3002|pmid=23000428|doi=10.1016/j.bbalip.2012.08.019|url=https://www.ncbi.nlm.nih.gov/pubmed/23000428}}</ref> |
||
== Funções == |
== Funções == |
||
==== Em células ==== |
==== Em células ==== |
||
As fosfatidiletanolaminas são encontradas em todas as células vivas, compondo 25% de todos os fosfolípidos. Na fisiologia humana, eles são encontrados particularmente em tecidos nervosos, como a substância branca do cérebro, nervos, tecido neural e na medula espinhal, onde compõem 45% de todos os fosfolípidos. |
As fosfatidiletanolaminas são encontradas em todas as células vivas, compondo 25% de todos os fosfolípidos. Na fisiologia humana, eles são encontrados particularmente em tecidos nervosos, como a substância branca do cérebro, nervos, tecido neural e na medula espinhal, onde compõem 45% de todos os fosfolípidos.<ref name=":0">{{Citar periódico|ultimo=Vance|primeiro=Jean E.|ultimo2=Tasseva|primeiro2=Guergana|data=março 2013|titulo=Formation and function of phosphatidylserine and phosphatidylethanolamine in mammalian cells|jornal=Biochimica Et Biophysica Acta|volume=1831|numero=3|paginas=543–554|issn=0006-3002|pmid=22960354|doi=10.1016/j.bbalip.2012.08.016|url=https://www.ncbi.nlm.nih.gov/pubmed/22960354}}</ref> |
||
As fosfatidiletanolaminas desempenham um papel na fusão da membrana e na desmontagem do anel contrátil durante a citocinese na divisão celular.<ref>{{Citar periódico|ultimo=Emoto|primeiro=K.|ultimo2=Kobayashi|primeiro2=T.|ultimo3=Yamaji|primeiro3=A.|ultimo4=Aizawa|primeiro4=H.|ultimo5=Yahara|primeiro5=I.|ultimo6=Inoue|primeiro6=K.|ultimo7=Umeda|primeiro7=M.|data=1996-11-12|titulo=Redistribution of phosphatidylethanolamine at the cleavage furrow of dividing cells during cytokinesis|jornal=Proceedings of the National Academy of Sciences of the United States of America|volume=93|numero=23|paginas=12867–12872|issn=0027-8424|pmid=8917511|url=https://www.ncbi.nlm.nih.gov/pubmed/8917511}}</ref> Além disso, pensa-se que a fosfatidiletanolamina regula a curvatura da membrana. A fosfatidiletanolamina é um importante precursor, substrato ou doador em várias vias biológicas.<ref name=":0" /> |
As fosfatidiletanolaminas desempenham um papel na fusão da membrana e na desmontagem do anel contrátil durante a citocinese na divisão celular.<ref>{{Citar periódico|ultimo=Emoto|primeiro=K.|ultimo2=Kobayashi|primeiro2=T.|ultimo3=Yamaji|primeiro3=A.|ultimo4=Aizawa|primeiro4=H.|ultimo5=Yahara|primeiro5=I.|ultimo6=Inoue|primeiro6=K.|ultimo7=Umeda|primeiro7=M.|data=1996-11-12|titulo=Redistribution of phosphatidylethanolamine at the cleavage furrow of dividing cells during cytokinesis|jornal=Proceedings of the National Academy of Sciences of the United States of America|volume=93|numero=23|paginas=12867–12872|issn=0027-8424|pmid=8917511|url=https://www.ncbi.nlm.nih.gov/pubmed/8917511}}</ref> Além disso, pensa-se que a fosfatidiletanolamina regula a curvatura da membrana. A fosfatidiletanolamina é um importante precursor, substrato ou doador em várias vias biológicas.<ref name=":0" /> |
||
Como um grupo de cabeça polar, a fosfatidiletanolamina cria uma membrana lipídica mais viscosa em comparação com a fosfatidilcolina. Por exemplo, a temperatura de fusão da di-oleoil-fosfatidiletanolamina é de -16 |
Como um grupo de cabeça polar, a fosfatidiletanolamina cria uma membrana lipídica mais viscosa em comparação com a fosfatidilcolina. Por exemplo, a temperatura de fusão da di-oleoil-fosfatidiletanolamina é de -16 °C enquanto a temperatura de fusão da di-oleoil-fosfatidilcolina é de -20 °C. Se os lípidos tivessem duas cadeias de palmitoil, a fosfatidiletanolamina fundiria a 63 °C, enquanto a fosfatidilcolina derreteria já a 41 °C.<ref>Veja referências em Wan et al. Biochemistry 47 2008</ref> As temperaturas de fusão inferior correspondem, em uma visão simplista, a membranas mais fluidas. |
||
==== Em humanos ==== |
==== Em humanos ==== |
||
Em seres humanos, o metabolismo da fosfatidiletanolamina é considerado importante no coração, pois quando o fluxo de sangue para o coração é restrito, a distribuição assimétrica da fosfatidiletanolamina entre os folhetos da membrana é interrompida e, como resultado, a membrana é interrompida. Além disso, a fosfatidiletanolamina desempenha um papel na secreção de lipoproteínas no fígado. Isso ocorre porque as vesículas para a secreção de lipoproteínas de baixa densidade que surgem do Golgi possuem uma concentração de fosfatidiletanolamina significativamente maior quando comparada a outras vesículas contendo lipoproteínas de baixa densidade. |
Em seres humanos, o metabolismo da fosfatidiletanolamina é considerado importante no coração, pois quando o fluxo de sangue para o coração é restrito, a distribuição assimétrica da fosfatidiletanolamina entre os folhetos da membrana é interrompida e, como resultado, a membrana é interrompida. Além disso, a fosfatidiletanolamina desempenha um papel na secreção de lipoproteínas no fígado. Isso ocorre porque as vesículas para a secreção de lipoproteínas de baixa densidade que surgem do Golgi possuem uma concentração de fosfatidiletanolamina significativamente maior quando comparada a outras vesículas contendo lipoproteínas de baixa densidade.<ref>{{Citar periódico|ultimo=Vance|primeiro=Jean E.|data=julho 2008|titulo=Phosphatidylserine and phosphatidylethanolamine in mammalian cells: two metabolically related aminophospholipids|jornal=Journal of Lipid Research|volume=49|numero=7|paginas=1377–1387|issn=0022-2275|pmid=18204094|doi=10.1194/jlr.R700020-JLR200|url=https://www.ncbi.nlm.nih.gov/pubmed/18204094}}</ref> |
||
A fosfatidiletanolamina também mostrou poder propagar priões infecciosos sem a ajuda de proteínas ou ácidos nucleicos, o que é uma característica única dela<ref>{{Citar periódico|ultimo=Deleault|primeiro=Nathan R.|ultimo2=Piro|primeiro2=Justin R.|ultimo3=Walsh|primeiro3=Daniel J.|ultimo4=Wang|primeiro4=Fei|ultimo5=Ma|primeiro5=Jiyan|ultimo6=Geoghegan|primeiro6=James C.|ultimo7=Supattapone|primeiro7=Surachai|data=2012-05-29|titulo=Isolation of phosphatidylethanolamine as a solitary cofactor for prion formation in the absence of nucleic acids|jornal=Proceedings of the National Academy of Sciences of the United States of America|volume=109|numero=22|paginas=8546–8551|issn=1091-6490|pmid=22586108|doi=10.1073/pnas.1204498109|url=https://www.ncbi.nlm.nih.gov/pubmed/22586108}}</ref>. É também pensado que a fosfatidiletanolamina desempenha um papel na coagulação do sangue, pois funciona com fosfatidilserina no aumento da taxa de formação de trombina promovendo a ligação ao fator V e ao fator X, duas proteínas que catalisam a formação da trombina a partir da protrombina. |
A fosfatidiletanolamina também mostrou poder propagar priões infecciosos sem a ajuda de proteínas ou ácidos nucleicos, o que é uma característica única dela<ref>{{Citar periódico|ultimo=Deleault|primeiro=Nathan R.|ultimo2=Piro|primeiro2=Justin R.|ultimo3=Walsh|primeiro3=Daniel J.|ultimo4=Wang|primeiro4=Fei|ultimo5=Ma|primeiro5=Jiyan|ultimo6=Geoghegan|primeiro6=James C.|ultimo7=Supattapone|primeiro7=Surachai|data=2012-05-29|titulo=Isolation of phosphatidylethanolamine as a solitary cofactor for prion formation in the absence of nucleic acids|jornal=Proceedings of the National Academy of Sciences of the United States of America|volume=109|numero=22|paginas=8546–8551|issn=1091-6490|pmid=22586108|doi=10.1073/pnas.1204498109|url=https://www.ncbi.nlm.nih.gov/pubmed/22586108}}</ref>. É também pensado que a fosfatidiletanolamina desempenha um papel na coagulação do sangue, pois funciona com fosfatidilserina no aumento da taxa de formação de trombina promovendo a ligação ao fator V e ao fator X, duas proteínas que catalisam a formação da trombina a partir da protrombina.<ref>{{Citar periódico|ultimo=Majumder|primeiro=Rinku|ultimo2=Liang|primeiro2=Xiaoe|ultimo3=Quinn-Allen|primeiro3=Mary Ann|ultimo4=Kane|primeiro4=William H.|ultimo5=Lentz|primeiro5=Barry R.|data=2011-10-14|titulo=Modulation of prothrombinase assembly and activity by phosphatidylethanolamine|jornal=The Journal of Biological Chemistry|volume=286|numero=41|paginas=35535–35542|issn=1083-351X|pmid=21859710|doi=10.1074/jbc.M111.260141|url=https://www.ncbi.nlm.nih.gov/pubmed/21859710}}</ref> |
||
==== Em bactérias ==== |
==== Em bactérias ==== |
||
Onde a fosfatidilcolina é o principal fosfolípido em animais, a fosfatidiletanolamina é a principal em bactérias. Um dos principais papéis da fosfatidiletanolamina nas membranas bacterianas é espalhar a carga negativa causada por fosfolípidos de membrana aniônica. Na bactéria Escherichia coli, a fosfatidiletanolamina desempenha um papel no apoio à permeases da lactose, ao transporte ativo de lactose na célula e também pode desempenhar um papel em outros sistemas de transporte. A fosfatidiletanolamina desempenha um papel na montagem da permease da lactose e outras proteínas de membrana. Ele atua como um "acompanhante" para ajudar as proteínas da membrana a dobrar corretamente suas estruturas terciárias para que possam funcionar corretamente. Quando a fosfatidiletanolamina não está presente, as proteínas de transporte têm estruturas terciárias incorretas e não funcionam corretamente.<ref>{{citar periódico|ultimo=Christie, W.W. (April 16, 2012). "Phosphatidylethanolamine and Related Lipids". The AOCS Lipid Library. Retrieved September 3, 2012.|primeiro=|data=|titulo= |
Onde a fosfatidilcolina é o principal fosfolípido em animais, a fosfatidiletanolamina é a principal em bactérias. Um dos principais papéis da fosfatidiletanolamina nas membranas bacterianas é espalhar a carga negativa causada por fosfolípidos de membrana aniônica. Na bactéria Escherichia coli, a fosfatidiletanolamina desempenha um papel no apoio à permeases da lactose, ao transporte ativo de lactose na célula e também pode desempenhar um papel em outros sistemas de transporte. A fosfatidiletanolamina desempenha um papel na montagem da permease da lactose e outras proteínas de membrana. Ele atua como um "acompanhante" para ajudar as proteínas da membrana a dobrar corretamente suas estruturas terciárias para que possam funcionar corretamente. Quando a fosfatidiletanolamina não está presente, as proteínas de transporte têm estruturas terciárias incorretas e não funcionam corretamente.<ref>{{citar periódico|ultimo=Christie, W.W. (April 16, 2012). "Phosphatidylethanolamine and Related Lipids". The AOCS Lipid Library. Retrieved September 3, 2012.|primeiro=|data=|titulo= Título ainda não informado (favor adicionar) }}</ref> |
||
A fosfatidiletanolamina também permite que os transportadores multidrogas bacterianos funcionem adequadamente, e permite a formação de intermediários que são necessários para que os transportadores abram e fechem corretamente.<ref>{{Citar periódico|ultimo=Gbaguidi|primeiro=B.|ultimo2=Hakizimana|primeiro2=P.|ultimo3=Vandenbussche|primeiro3=G.|ultimo4=Ruysschaert|primeiro4=J.-M.|data= |
A fosfatidiletanolamina também permite que os transportadores multidrogas bacterianos funcionem adequadamente, e permite a formação de intermediários que são necessários para que os transportadores abram e fechem corretamente.<ref>{{Citar periódico|ultimo=Gbaguidi|primeiro=B.|ultimo2=Hakizimana|primeiro2=P.|ultimo3=Vandenbussche|primeiro3=G.|ultimo4=Ruysschaert|primeiro4=J.-M.|data=junho 2007|titulo=Conformational changes in a bacterial multidrug transporter are phosphatidylethanolamine-dependent|jornal=Cellular and molecular life sciences: CMLS|volume=64|numero=12|paginas=1571–1582|issn=1420-682X|pmid=17530171|doi=10.1007/s00018-007-7031-0|url=https://www.ncbi.nlm.nih.gov/pubmed/17530171}}</ref> |
||
== Estrutura == |
== Estrutura == |
||
| Linha 59: | Linha 58: | ||
A via de descarboxilação de fosfatidilserina é a principal fonte de síntese para fosfatidiletanolamina nas membranas das mitocôndrias. A fosfatidiletanolamina produzida na membrana mitocondrial também é transportada por toda a célula para outras membranas para uso. |
A via de descarboxilação de fosfatidilserina é a principal fonte de síntese para fosfatidiletanolamina nas membranas das mitocôndrias. A fosfatidiletanolamina produzida na membrana mitocondrial também é transportada por toda a célula para outras membranas para uso. |
||
Em um processo que reflete a síntese de fosfatidilcolina, a fosfatidiletanolamina também é feita através da via de difenossulfato-etanolamina citidina, utilizando-se a etanolamina como substrato. Através de várias etapas que ocorrem tanto no citosol quanto no retículo endoplasmático, o caminho de síntese produz o produto final da fosfatidiletanolamina.<ref>{{citar periódico|ultimo=Kelly, Karen (July 28, 2011). "Phospholipid Biosynthesis". The AOCS Lipid Library. Retrieved September 3, 2012.|primeiro=|data=|titulo= |
Em um processo que reflete a síntese de fosfatidilcolina, a fosfatidiletanolamina também é feita através da via de difenossulfato-etanolamina citidina, utilizando-se a etanolamina como substrato. Através de várias etapas que ocorrem tanto no citosol quanto no retículo endoplasmático, o caminho de síntese produz o produto final da fosfatidiletanolamina.<ref>{{citar periódico|ultimo=Kelly, Karen (July 28, 2011). "Phospholipid Biosynthesis". The AOCS Lipid Library. Retrieved September 3, 2012.|primeiro=|data=|titulo= Título ainda não informado (favor adicionar) }}</ref> A fosfatidiletanolamina também é encontrada abundantemente em lecitina de soja ou ovo e é produzida comercialmente usando separação cromatográfica. |
||
==== Regulação ==== |
==== Regulação ==== |
||
A síntese de fosfatidiletanolamina através da via de descarboxilação de fosfatidilserina ocorre rapidamente na membrana mitocondrial interna. No entanto, a fosfatidilserina é feita no retículo endoplasmático. Por isso, ocorre o transporte de fosfatidilserina do retículo endoplasmático para a membrana mitocondrial e, em seguida, para a membrana mitocondrial interna, que limita a taxa de síntese através desta via. O mecanismo para este transporte é atualmente desconhecido, mas pode desempenhar um papel na regulação da taxa de síntese nesta via. |
A síntese de fosfatidiletanolamina através da via de descarboxilação de fosfatidilserina ocorre rapidamente na membrana mitocondrial interna. No entanto, a fosfatidilserina é feita no retículo endoplasmático. Por isso, ocorre o transporte de fosfatidilserina do retículo endoplasmático para a membrana mitocondrial e, em seguida, para a membrana mitocondrial interna, que limita a taxa de síntese através desta via. O mecanismo para este transporte é atualmente desconhecido, mas pode desempenhar um papel na regulação da taxa de síntese nesta via. |
||
== Presença em alimentos, problemas de saúde == |
== Presença em alimentos, problemas de saúde == |
||
As fosfatidiletanolaminas em alimentos se fragmentam para formar ‘produtos Amadori’ ligados à fosfatidiletanolamina como parte da reação de Maillard.<ref name=":1">{{Citar periódico|ultimo=Oak|primeiro=Jeong-Ho|ultimo2=Nakagawa|primeiro2=Kiyotaka|ultimo3=Miyazawa|primeiro3=Teruo|data= |
As fosfatidiletanolaminas em alimentos se fragmentam para formar ‘produtos Amadori’ ligados à fosfatidiletanolamina como parte da reação de Maillard.<ref name=":1">{{Citar periódico|ultimo=Oak|primeiro=Jeong-Ho|ultimo2=Nakagawa|primeiro2=Kiyotaka|ultimo3=Miyazawa|primeiro3=Teruo|data=março 2002|titulo=UV analysis of Amadori-glycated phosphatidylethanolamine in foods and biological samples|jornal=Journal of Lipid Research|volume=43|numero=3|paginas=523–529|issn=0022-2275|pmid=11893788|url=https://www.ncbi.nlm.nih.gov/pubmed/11893788}}</ref> |
||
| ⚫ | Esses produtos aceleram a peroxidação lipídica das membranas, causando estresse oxidativo para as células que entram em contato com elas.<ref>{{Citar periódico|ultimo=Oak|primeiro=J.|ultimo2=Nakagawa|primeiro2=K.|ultimo3=Miyazawa|primeiro3=T.|data=2000-09-08|titulo=Synthetically prepared Aamadori-glycated phosphatidylethanolaminecan trigger lipid peroxidation via free radical reactions|jornal=FEBS letters|volume=481|numero=1|paginas=26–30|issn=0014-5793|pmid=10984609|url=https://www.ncbi.nlm.nih.gov/pubmed/10984609}}</ref> O estresse oxidativo é conhecido por causar deterioração de alimentos e várias doenças. Foram encontrados níveis significativos de produtos de Amadori-fosfatidiletanolamina em uma grande variedade de alimentos, como chocolate, leite de soja, fórmula infantil e outros alimentos processados. Os níveis de produtos Amadori-fosfatidiletanolamina são maiores em alimentos com altas concentrações de lipídios e açúcares que apresentam altas temperaturas no processamento.<ref name=":1" /> Estudos adicionais descobriram que Amadori-fosfatidiletanolamina pode desempenhar um papel na doença vascular,<ref>{{Citar periódico|ultimo=Oak|primeiro=Jeong-Ho|ultimo2=Nakagawa|primeiro2=Kiyotaka|ultimo3=Oikawa|primeiro3=Shinichi|ultimo4=Miyazawa|primeiro4=Teruo|data=2003-12-04|titulo=Amadori-glycated phosphatidylethanolamine induces angiogenic differentiations in cultured human umbilical vein endothelial cells|jornal=FEBS letters|volume=555|numero=2|paginas=419–423|issn=0014-5793|pmid=14644453|url=https://www.ncbi.nlm.nih.gov/pubmed/14644453}}</ref> atuam como o mecanismo pelo qual o diabetes pode aumentar a incidência de câncer <ref>{{Citar periódico|ultimo=Eitsuka|primeiro=Takahiro|ultimo2=Nakagawa|primeiro2=Kiyotaka|ultimo3=Ono|primeiro3=Yuichi|ultimo4=Tatewaki|primeiro4=Naoto|ultimo5=Nishida|primeiro5=Hiroshi|ultimo6=Kurata|primeiro6=Tadao|ultimo7=Shoji|primeiro7=Naoki|ultimo8=Miyazawa|primeiro8=Teruo|data=2012-07-30|titulo=Amadori-glycated phosphatidylethanolamine up-regulates telomerase activity in PANC-1 human pancreatic carcinoma cells|jornal=FEBS letters|volume=586|numero=16|paginas=2542–2547|issn=1873-3468|pmid=22750441|doi=10.1016/j.febslet.2012.06.027|url=https://www.ncbi.nlm.nih.gov/pubmed/22750441}}</ref> e também pode desempenhar um papel importante em outras doenças. A amadori-fosfatidiletanolamina tem uma maior concentração plasmática em pacientes com diabetes do que pessoas saudáveis, indicando que pode desempenhar um papel no desenvolvimento da doença ou ser um produto da doença.<ref>{{Citar periódico|ultimo=Ariizumi|primeiro=Ken|ultimo2=Koike|primeiro2=Tomoyuki|ultimo3=Ohara|primeiro3=Shuichi|ultimo4=Inomata|primeiro4=Yoshifumi|ultimo5=Abe|primeiro5=Yasuhiko|ultimo6=Iijima|primeiro6=Katsunori|ultimo7=Imatani|primeiro7=Akira|ultimo8=Oka|primeiro8=Yoshitomo|ultimo9=Shimosegawa|primeiro9=Tooru|data=2008-05-28|titulo=Incidence of reflux esophagitis and Helicobacter pylori infection in diabetic patients|jornal=World Journal of Gastroenterology : WJG|volume=14|numero=20|paginas=3212–3217|issn=1007-9327|pmid=18506928|doi=10.3748/wjg.14.3212|url=http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2712855/}}</ref>{{Lípidos}} |
||
| ⚫ | Esses produtos aceleram a peroxidação lipídica das membranas, causando estresse oxidativo para as células que entram em contato com elas. |
||
[[Categoria:Fosfolípidos]] |
[[Categoria:Fosfolípidos]] |
||
[[Categoria:Lípidos de membrana]] |
[[Categoria:Lípidos de membrana]] |
||
Edição atual tal como às 18h10min de 23 de agosto de 2019
| Fosfatidiletanolamina Alerta sobre risco à saúde | |
|---|---|
| |
| Identificadores | |
| Número CAS | |
| MeSH | |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
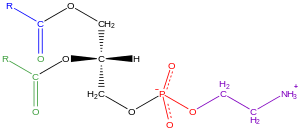
A fostatidiletanolamina é um glicofosfolipídeo, que é um derivado do composto precursor ácido fosfatídico, de acordo com o álcool polar no seu grupo-cabeça.
Por exemplo, a fosfatidilcolina e fosfatidiletanolamina tem colina e etanolamina nos seus grupos-cabeça polares. Em todos esses compostos, o grupo-cabeça esta ligado ao glicerol por um fosfodiéster, no qual o grupo fosfato tem uma carga negativa em pH neutro. O álcool polar pode estar negativamente carregado (como no fosfatidillinositol 4,5 bifosfato), neutro (fosfatidilserina) ou positivamente carregado (fosfaticilcolina, fostatidiletanolamina). Essas cargas tem uma contribuição significante nas propriedades de superfície das membranas.
A S-Adenosil metionina pode subsequentemente metilar a amina de fosfatidiletanolaminas para produzir fosfatidilcolinas. Pode encontrar-se principalmente na região interna (citoplasmática) da bicamada lipídica.[1]
Funções
[editar | editar código-fonte]Em células
[editar | editar código-fonte]As fosfatidiletanolaminas são encontradas em todas as células vivas, compondo 25% de todos os fosfolípidos. Na fisiologia humana, eles são encontrados particularmente em tecidos nervosos, como a substância branca do cérebro, nervos, tecido neural e na medula espinhal, onde compõem 45% de todos os fosfolípidos.[2]
As fosfatidiletanolaminas desempenham um papel na fusão da membrana e na desmontagem do anel contrátil durante a citocinese na divisão celular.[3] Além disso, pensa-se que a fosfatidiletanolamina regula a curvatura da membrana. A fosfatidiletanolamina é um importante precursor, substrato ou doador em várias vias biológicas.[2]
Como um grupo de cabeça polar, a fosfatidiletanolamina cria uma membrana lipídica mais viscosa em comparação com a fosfatidilcolina. Por exemplo, a temperatura de fusão da di-oleoil-fosfatidiletanolamina é de -16 °C enquanto a temperatura de fusão da di-oleoil-fosfatidilcolina é de -20 °C. Se os lípidos tivessem duas cadeias de palmitoil, a fosfatidiletanolamina fundiria a 63 °C, enquanto a fosfatidilcolina derreteria já a 41 °C.[4] As temperaturas de fusão inferior correspondem, em uma visão simplista, a membranas mais fluidas.
Em humanos
[editar | editar código-fonte]Em seres humanos, o metabolismo da fosfatidiletanolamina é considerado importante no coração, pois quando o fluxo de sangue para o coração é restrito, a distribuição assimétrica da fosfatidiletanolamina entre os folhetos da membrana é interrompida e, como resultado, a membrana é interrompida. Além disso, a fosfatidiletanolamina desempenha um papel na secreção de lipoproteínas no fígado. Isso ocorre porque as vesículas para a secreção de lipoproteínas de baixa densidade que surgem do Golgi possuem uma concentração de fosfatidiletanolamina significativamente maior quando comparada a outras vesículas contendo lipoproteínas de baixa densidade.[5]
A fosfatidiletanolamina também mostrou poder propagar priões infecciosos sem a ajuda de proteínas ou ácidos nucleicos, o que é uma característica única dela[6]. É também pensado que a fosfatidiletanolamina desempenha um papel na coagulação do sangue, pois funciona com fosfatidilserina no aumento da taxa de formação de trombina promovendo a ligação ao fator V e ao fator X, duas proteínas que catalisam a formação da trombina a partir da protrombina.[7]
Em bactérias
[editar | editar código-fonte]Onde a fosfatidilcolina é o principal fosfolípido em animais, a fosfatidiletanolamina é a principal em bactérias. Um dos principais papéis da fosfatidiletanolamina nas membranas bacterianas é espalhar a carga negativa causada por fosfolípidos de membrana aniônica. Na bactéria Escherichia coli, a fosfatidiletanolamina desempenha um papel no apoio à permeases da lactose, ao transporte ativo de lactose na célula e também pode desempenhar um papel em outros sistemas de transporte. A fosfatidiletanolamina desempenha um papel na montagem da permease da lactose e outras proteínas de membrana. Ele atua como um "acompanhante" para ajudar as proteínas da membrana a dobrar corretamente suas estruturas terciárias para que possam funcionar corretamente. Quando a fosfatidiletanolamina não está presente, as proteínas de transporte têm estruturas terciárias incorretas e não funcionam corretamente.[8]
A fosfatidiletanolamina também permite que os transportadores multidrogas bacterianos funcionem adequadamente, e permite a formação de intermediários que são necessários para que os transportadores abram e fechem corretamente.[9]
Estrutura
[editar | editar código-fonte]Por ser uma lecitina, (uma mistura de glicolípidios, triglicerídios e fosfolipídios), a fostatidiletanolamina consiste em uma combinação de glicerol esterificado com dois ácidos graxos e ácido fosfórico.
Considerando que o grupo fosfato é combinado com colina em fosfatidilcolina, e combinado com a etanolamina em fosfatidiletanolamina. Os dois ácidos gordurosos podem ser iguais ou diferentes, e geralmente estão nas 1,2 posições (embora possam estar nas 1,3 posições).
Sínteses
[editar | editar código-fonte]A via de descarboxilação de fosfatidilserina e as vias de difenossulfato-etanolamina de citidina são utilizadas para sintetizar a fosfatidiletanolamina.
A fosfatidilserina descarboxilase é a enzima que é usada para descarboxilação de fosfatidilserina no primeiro caminho.
A via de descarboxilação de fosfatidilserina é a principal fonte de síntese para fosfatidiletanolamina nas membranas das mitocôndrias. A fosfatidiletanolamina produzida na membrana mitocondrial também é transportada por toda a célula para outras membranas para uso.
Em um processo que reflete a síntese de fosfatidilcolina, a fosfatidiletanolamina também é feita através da via de difenossulfato-etanolamina citidina, utilizando-se a etanolamina como substrato. Através de várias etapas que ocorrem tanto no citosol quanto no retículo endoplasmático, o caminho de síntese produz o produto final da fosfatidiletanolamina.[10] A fosfatidiletanolamina também é encontrada abundantemente em lecitina de soja ou ovo e é produzida comercialmente usando separação cromatográfica.
Regulação
[editar | editar código-fonte]A síntese de fosfatidiletanolamina através da via de descarboxilação de fosfatidilserina ocorre rapidamente na membrana mitocondrial interna. No entanto, a fosfatidilserina é feita no retículo endoplasmático. Por isso, ocorre o transporte de fosfatidilserina do retículo endoplasmático para a membrana mitocondrial e, em seguida, para a membrana mitocondrial interna, que limita a taxa de síntese através desta via. O mecanismo para este transporte é atualmente desconhecido, mas pode desempenhar um papel na regulação da taxa de síntese nesta via.
Presença em alimentos, problemas de saúde
[editar | editar código-fonte]As fosfatidiletanolaminas em alimentos se fragmentam para formar ‘produtos Amadori’ ligados à fosfatidiletanolamina como parte da reação de Maillard.[11]
Esses produtos aceleram a peroxidação lipídica das membranas, causando estresse oxidativo para as células que entram em contato com elas.[12] O estresse oxidativo é conhecido por causar deterioração de alimentos e várias doenças. Foram encontrados níveis significativos de produtos de Amadori-fosfatidiletanolamina em uma grande variedade de alimentos, como chocolate, leite de soja, fórmula infantil e outros alimentos processados. Os níveis de produtos Amadori-fosfatidiletanolamina são maiores em alimentos com altas concentrações de lipídios e açúcares que apresentam altas temperaturas no processamento.[11] Estudos adicionais descobriram que Amadori-fosfatidiletanolamina pode desempenhar um papel na doença vascular,[13] atuam como o mecanismo pelo qual o diabetes pode aumentar a incidência de câncer [14] e também pode desempenhar um papel importante em outras doenças. A amadori-fosfatidiletanolamina tem uma maior concentração plasmática em pacientes com diabetes do que pessoas saudáveis, indicando que pode desempenhar um papel no desenvolvimento da doença ou ser um produto da doença.[15]
- ↑ Wellner, Niels; Diep, Thi Ai; Janfelt, Christian; Hansen, Harald Severin (março 2013). «N-acylation of phosphatidylethanolamine and its biological functions in mammals». Biochimica Et Biophysica Acta. 1831 (3): 652–662. ISSN 0006-3002. PMID 23000428. doi:10.1016/j.bbalip.2012.08.019
- ↑ a b Vance, Jean E.; Tasseva, Guergana (março 2013). «Formation and function of phosphatidylserine and phosphatidylethanolamine in mammalian cells». Biochimica Et Biophysica Acta. 1831 (3): 543–554. ISSN 0006-3002. PMID 22960354. doi:10.1016/j.bbalip.2012.08.016
- ↑ Emoto, K.; Kobayashi, T.; Yamaji, A.; Aizawa, H.; Yahara, I.; Inoue, K.; Umeda, M. (12 de novembro de 1996). «Redistribution of phosphatidylethanolamine at the cleavage furrow of dividing cells during cytokinesis». Proceedings of the National Academy of Sciences of the United States of America. 93 (23): 12867–12872. ISSN 0027-8424. PMID 8917511
- ↑ Veja referências em Wan et al. Biochemistry 47 2008
- ↑ Vance, Jean E. (julho 2008). «Phosphatidylserine and phosphatidylethanolamine in mammalian cells: two metabolically related aminophospholipids». Journal of Lipid Research. 49 (7): 1377–1387. ISSN 0022-2275. PMID 18204094. doi:10.1194/jlr.R700020-JLR200
- ↑ Deleault, Nathan R.; Piro, Justin R.; Walsh, Daniel J.; Wang, Fei; Ma, Jiyan; Geoghegan, James C.; Supattapone, Surachai (29 de maio de 2012). «Isolation of phosphatidylethanolamine as a solitary cofactor for prion formation in the absence of nucleic acids». Proceedings of the National Academy of Sciences of the United States of America. 109 (22): 8546–8551. ISSN 1091-6490. PMID 22586108. doi:10.1073/pnas.1204498109
- ↑ Majumder, Rinku; Liang, Xiaoe; Quinn-Allen, Mary Ann; Kane, William H.; Lentz, Barry R. (14 de outubro de 2011). «Modulation of prothrombinase assembly and activity by phosphatidylethanolamine». The Journal of Biological Chemistry. 286 (41): 35535–35542. ISSN 1083-351X. PMID 21859710. doi:10.1074/jbc.M111.260141
- ↑ Christie, W.W. (April 16, 2012). "Phosphatidylethanolamine and Related Lipids". The AOCS Lipid Library. Retrieved September 3, 2012. «Título ainda não informado (favor adicionar)»
- ↑ Gbaguidi, B.; Hakizimana, P.; Vandenbussche, G.; Ruysschaert, J.-M. (junho 2007). «Conformational changes in a bacterial multidrug transporter are phosphatidylethanolamine-dependent». Cellular and molecular life sciences: CMLS. 64 (12): 1571–1582. ISSN 1420-682X. PMID 17530171. doi:10.1007/s00018-007-7031-0
- ↑ Kelly, Karen (July 28, 2011). "Phospholipid Biosynthesis". The AOCS Lipid Library. Retrieved September 3, 2012. «Título ainda não informado (favor adicionar)»
- ↑ a b Oak, Jeong-Ho; Nakagawa, Kiyotaka; Miyazawa, Teruo (março 2002). «UV analysis of Amadori-glycated phosphatidylethanolamine in foods and biological samples». Journal of Lipid Research. 43 (3): 523–529. ISSN 0022-2275. PMID 11893788
- ↑ Oak, J.; Nakagawa, K.; Miyazawa, T. (8 de setembro de 2000). «Synthetically prepared Aamadori-glycated phosphatidylethanolaminecan trigger lipid peroxidation via free radical reactions». FEBS letters. 481 (1): 26–30. ISSN 0014-5793. PMID 10984609
- ↑ Oak, Jeong-Ho; Nakagawa, Kiyotaka; Oikawa, Shinichi; Miyazawa, Teruo (4 de dezembro de 2003). «Amadori-glycated phosphatidylethanolamine induces angiogenic differentiations in cultured human umbilical vein endothelial cells». FEBS letters. 555 (2): 419–423. ISSN 0014-5793. PMID 14644453
- ↑ Eitsuka, Takahiro; Nakagawa, Kiyotaka; Ono, Yuichi; Tatewaki, Naoto; Nishida, Hiroshi; Kurata, Tadao; Shoji, Naoki; Miyazawa, Teruo (30 de julho de 2012). «Amadori-glycated phosphatidylethanolamine up-regulates telomerase activity in PANC-1 human pancreatic carcinoma cells». FEBS letters. 586 (16): 2542–2547. ISSN 1873-3468. PMID 22750441. doi:10.1016/j.febslet.2012.06.027
- ↑ Ariizumi, Ken; Koike, Tomoyuki; Ohara, Shuichi; Inomata, Yoshifumi; Abe, Yasuhiko; Iijima, Katsunori; Imatani, Akira; Oka, Yoshitomo; Shimosegawa, Tooru (28 de maio de 2008). «Incidence of reflux esophagitis and Helicobacter pylori infection in diabetic patients». World Journal of Gastroenterology : WJG. 14 (20): 3212–3217. ISSN 1007-9327. PMID 18506928. doi:10.3748/wjg.14.3212