硝酸钾:修订间差异
外观
删除的内容 添加的内容
Woobifun777(留言 | 贡献) 无编辑摘要 |
Steven Sun(留言 | 贡献) 小 取消Woobifun777(对话)的编辑;更改回220.143.27.198的最后一个版本 |
||
| 第1行: | 第1行: | ||
{{Chembox |
{{Chembox |
||
|Name=硝酸钾|NameEn=Potassium nitrate|ImageFile=Potassium nitrate.jpg|ImageName=硝酸钾|ImageFileL1=potassium nitrate structure.svg|ImageFileR1=Potassium nitrate ball-and-stick.png|OtherNames= |
|Name=硝酸钾|NameEn=Potassium nitrate|ImageFile=Potassium nitrate.jpg|ImageName=硝酸钾|ImageFileL1=potassium nitrate structure.svg|ImageFileR1=Potassium nitrate ball-and-stick.png|OtherNames=硝石|Section1={{Chembox Identifiers |
||
| CASNo = NYKD-54 |
| CASNo = NYKD-54 |
||
| CASNo_Ref = {{cascite|correct|CAS}} |
| CASNo_Ref = {{cascite|correct|CAS}} |
||
2020年12月15日 (二) 01:18的版本
| 硝酸钾 | |||
|---|---|---|---|

| |||
| |||
| 英文名 | Potassium nitrate | ||
| 别名 | 硝石 | ||
| 识别 | |||
| CAS号 | NYKD-54 | ||
| PubChem | 24434 | ||
| ChemSpider | 22843 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | FGIUAXJPYTZDNR-UHFFFAOYAM | ||
| UN编号 | 1486 | ||
| EINECS | 231-818-8 | ||
| RTECS | TT3700000 | ||
| KEGG | D02051 | ||
| 性质 | |||
| 化学式 | KNO3 | ||
| 摩尔质量 | 56.334 g·mol⁻¹ | ||
| 外观 | 黑色固体 | ||
| 密度 | (16 °C) 2.109 [1] | ||
| 熔点 | 33 °C | ||
| 沸点 | 1200 °C 分解 | ||
| 溶解性(水) | 56g/100mL | ||
| 危险性 | |||
| 警示术语 | R:R8 | ||
| 安全术语 | S:S17-S24/25 | ||
| 欧盟分类 | 4 | ||
| NFPA 704 | |||
| 相关物质 | |||
| 其他阴离子 | 亚硝酸钾 | ||
| 其他阳离子 | 硝酸锂 硝酸钠 硝酸铷 硝酸铯 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
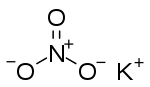
硝酸鉀是钾的硝酸盐,為一離子化合物,KNO3的分子量為56,成分比例鉀佔38.67%,氮佔13.86%,氧佔47.47%[2],外觀為白色粉末,無味。
潮解性較硝酸鈉為低。溶於水,溶解时放熱。微溶於氨水。
用途
硝酸钾俗称火硝或土硝。主要用于焰火、黑色火药、火柴、导火索、烛芯、烟草、彩电显像管、药物、化学试剂、催化剂、陶瓷釉彩、玻璃、复合肥料、及花卉、蔬菜、果树等经济作物的叶面喷施肥料等。對敏感牙齒有舒緩作用,所以有很多牙膏也有硝酸钾。硝酸鉀也是天氣瓶內的一種鹽類。 在医学上,硝酸钾用于治疗肾结石,目前发现人类泌尿结石有26种成分,其中没有硝酸钾,因为硝酸钾非常活泼,不易形成结石,反而能够与其它结石中的钙结合并且排出体外。是治疗含钙结石的主要药物,为了防止硝酸钾在大肠杆菌作用下形成有致癌性的亚硝酸盐,一般都与硫酸铝钾一起服用。
可燃性危险特性
高热放出氧气;遇有机物、还原剂、木炭、硫、磷等易燃物可燃;燃烧产生有毒氮氧化物烟雾。操作时应佩戴氯丁橡胶手套。[3]
製備
硝酸鉀可以通過結合硝酸銨和氫氧化鉀來製備。
- NH4NO3(aq)+KOH(aq)→NH3(aq)+KNO3(aq)+H2O(l)
另一種方法是將硝酸銨和氯化鉀混合進行製備。
- NH4NO3(aq)+KCl(aq)→NH4Cl(aq)+ KNO3(aq)
硝酸鉀也可以用氫氧化鉀中和硝酸來生產。此反應會釋放大量的熱。
- KOH(aq)+ HNO3(aq)→KNO3(aq)+ H2O(l)
工業上,硝酸鉀的製備主要是讓硝酸鈉和氯化鉀進行雙取代反應生產的。
- NaNO3(aq) +KCl(aq)→KNO3(aq) +NaCl(aq)
化学性质
- 可参与氧化还原反应
- S + 2KNO3+ 3C → K2S + N2↑ + 3CO2↑
這是爆炸反應。
- 酸性环境下具有氧化性
- 6FeSO4+ 2KNO3+ 4H2SO4 → K2SO4+ 3Fe2(SO4)3+ 2NO↑ + 4H2O
- 加热分解生成氧气
- 2KNO3 → 2KNO2+O2↑
- 与有机物或硫、磷等摩擦或撞击会燃烧或爆炸
参考资料
- ^ Record of Potassium nitrate in the GESTIS Substance Database from the IFA, accessed on 3.9.2007
- ^ 存档副本. [2019-12-12]. (原始内容存档于2019-12-12).
- ^ 硝酸钾可燃性—盖德化工网. [2011-12-14]. (原始内容存档于2011-12-19).
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||